Περισσότεροι από 700 επιστήμονες απ’ όλον τον κόσμο βρέθηκαν στην Αθήνα από τις 15 έως και τις 18 Οκτωβρίου προκειμένου να συμμετάσχουν στις εργασίες του ετήσιου συνεδρίου της Διεθνούς Εταιρείας Κυτταροκινών και Ιντερφερονών (International Cytokine and Interferons Society, ICIS). Ο τίτλος του συνεδρίου ήταν «Οι κυτταροκίνες και οι ιντερφερόνες στην εποχή της Ιατρικής Ακριβείας» και πρόεδρος της διοργάνωσής του ήταν ο δρ Ευάγγελος Ανδρεάκος, ερευνητής του Ιδρύματος Ιατροβιολογικών Ερευνών της Ακαδημίας Αθηνών (ΙΙΒΕΑΑ), συνεπικουρούμενος από τον δρα Γιώργο Παυλάκη, ερευνητή στα Εθνικά Ινστιτούτα Υγείας των ΗΠΑ. Το ΒΗΜΑ-Science παρακολούθησε τις εργασίες του συνεδρίου και σας μεταφέρει σήμερα μερικά από τα πολλά ενδιαφέροντα ευρήματα τα οποία παρουσιάστηκαν σε αυτό, με έμφαση στο πώς τα ερευνητικά ευρήματα «γεννούν» νέες καινοτόμες θεραπείες.

Ανοσορύθμιση
Τι είναι όμως οι κυτταροκίνες και οι ιντερφερόνες, για την έρευνα των οποίων έχει δημιουργηθεί μια ευρεία επιστημονική κοινότητα και οι οποίες, όπως αφήνεται να εννοηθεί από τον τίτλο του συνεδρίου, διαδραματίζουν κομβικό ρόλο στην ιατρική ακριβείας; Η ελληνική ρίζα της λέξης «κυτταροκίνες» (κύτταρο + κινώ) είναι αποκαλυπτική του ρόλου τους: πρόκειται για πρωτεϊνικά μόρια (σχετικά χαμηλού μοριακού βάρους) τα οποία έχουν ανοσορυθμιστικό ρόλο, κινητοποιούν δηλαδή τα κύτταρα του ανοσοποιητικού συστήματος να αναλάβουν δράση. Υποκατηγορία των κυτταροκινών είναι οι ιντερφερόνες (από την αγγλική λέξη «interfere», η οποία υποδηλώνει την ανάμειξη αυτών των μορίων σε πληθώρα κυτταρικών διεργασιών), αλλά και οι ιντερλευκίνες, οι λεμφοκίνες, οι χυμοκίνες και οι παράγοντες νέκρωσης όγκων.
Ευρεία δράση
Με δεδομένο ότι το ανθρώπινο ανοσοποιητικό σύστημα έχει σμιλευθεί εξελικτικά για να μας προστατεύει τόσο από εξωτερικούς εισβολείς (ιούς, βακτήρια, μύκητες) όσο και εσωτερικούς (καρκινικούς όγκους), γίνεται εύκολα αντιληπτό ότι οι κυτταροκίνες ως ανοσορυθμιστικά μόρια εμπλέκονται τόσο στα λοιμώδη νοσήματα όσο και στον καρκίνο.
Και καθώς η καλή λειτουργία του ανοσοποιητικού συστήματος δεν είναι πάντοτε δεδομένη, οι κυτταροκίνες παίζουν επίσης ρόλο στην εμφάνιση των αυτοάνοσων νοσημάτων (των νοσημάτων, δηλαδή, τα οποία προκύπτουν όταν ο οργανισμός αδυνατεί να αναγνωρίσει ως ίδια ορισμένα στοιχεία του εαυτού του και οργανώνει επίθεση εναντίον τους ως αυτά να ήταν ξένοι εισβολείς). Διόλου περίεργο λοιπόν το γεγονός ότι οι κυτταροκίνες, οι οποίες πρωτοανακαλύφθηκαν στα τέλη της δεκαετίας του 1950, όταν άρχισαν να μελετώνται και να γίνεται αντιληπτός ο ρόλος τους, αποτέλεσαν τη βάση για την ανάπτυξη μιας μεγάλης σειράς φαρμάκων, ο αριθμός των οποίων αυξάνει συνεχώς.
Οι κυτταροκίνες παράγονται και εκλύονται από διάφορα είδη κυττάρων (όχι μόνο του ανοσοποιητικού) και ασκούν τη δράση
τους προσδενόμενες σε υποδοχείς πάνω στην επιφάνεια των κυττάρων-στόχων τους
Καρκίνος
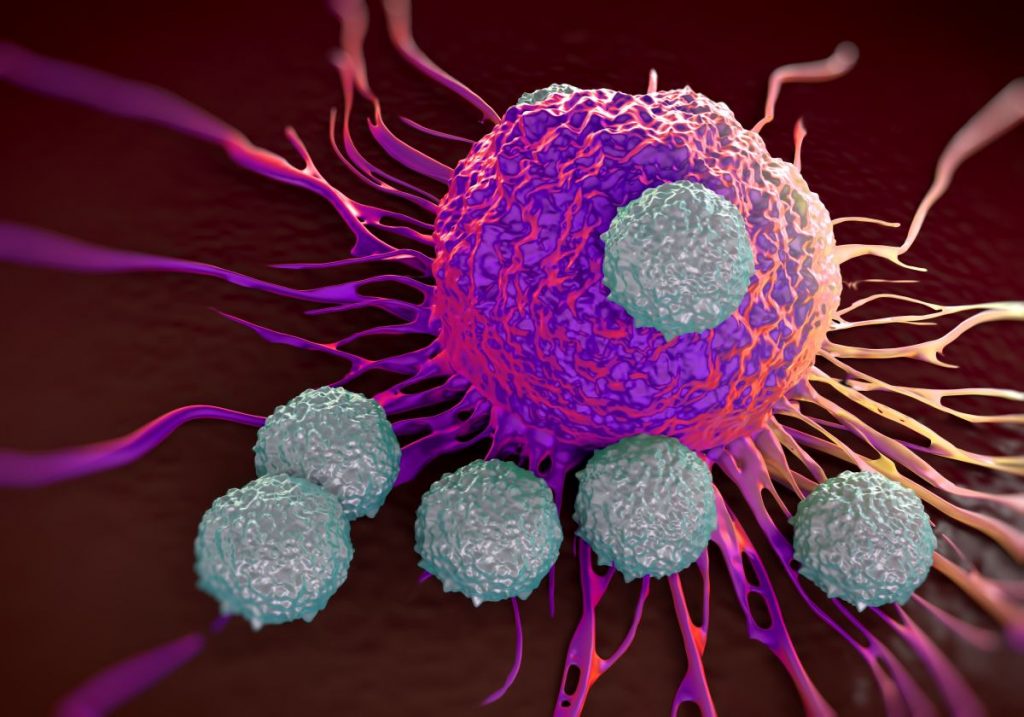
Η κακοήθης εξαλλαγή των κυττάρων είναι μια διαδικασία η οποία διεγείρει μεν το ανοσοποιητικό σύστημα, αλλά συχνά όχι σε βαθμό ικανό να αποτρέψει τον σχηματισμό των όγκων. Αυτό συμβαίνει (και) επειδή τα καρκινικά κύτταρα δημιουργούν γύρω τους ένα μικροπεριβάλλον που «ξεγελά» το ανοσοποιητικό σύστημα. Ειδικότερα, τα Τ κύτταρα φονείς του ανοσοποιητικού αναγνωρίζουν τους στόχους τους (καρκινικά κύτταρα, αλλά και μικροβιακά) μέσω μιας πολύ καλά ελεγχόμενης διαδικασίας τριών βημάτων, τα οποία εξασφαλίζουν ότι τα κύτταρα θα επιτεθούν εκεί που πρέπει για όσο χρόνο χρειάζεται, αλλά και ότι θα σταματήσουν την επίθεσή τους όταν πρέπει (βήμα 3). Αυτό το άρτια σχεδιασμένο εξελικτικά σύστημα προστασίας πετυχαίνει να ανατρέψει τα καρκινικά κύτταρα τα οποία παρεμποδίζουν τόσο την αρχική αναγνώρισή τους από τα Τ κύτταρα (βήμα 1) όσο και την ενίσχυση του πολλαπλασιασμού των εξειδικευμένων Τ κυττάρων (βήμα 2) τα οποία θα είχαν τη δυνατότητα να στραφούν εναντίον τους.
Δικλωνική υπεροχή
Στην ενίσχυση της προσπάθειας του ανοσοποιητικού συστήματος να αποτρέψει τον σχηματισμό των όγκων στοχεύει μια σειρά ήδη υπαρχόντων αντικαρκινικών φαρμάκων. Ωστόσο ετοιμάζεται μια νέα γενιά φαρμάκων τα οποία είναι δικλωνικά αντισώματα. Αντισώματα δηλαδή ειδικά σχεδιασμένα να αναγνωρίζουν δύο αντιγόνα. Οπως εξήγησε κατά τη διάρκεια της διάλεξής του στο συνέδριο ο επικεφαλής του τμήματος ογκολογίας της εταιρείας Regeneron στις ΗΠΑ, δρ Δημήτρης Σκόκος, «τα δικλωνικά αντισώματα έχουν σχεδιαστεί ώστε να αυξάνουν τη διάρκεια της αντίδρασης του ανοσοποιητικού συστήματος ενισχύοντας τα βήματα ένα και δύο.
Στην πραγματικότητα τα αντισώματα τα οποία σχεδιάζονται ώστε να αναγνωρίζουν στοιχεία των καρκινικών κυττάρων και των Τ κυττάρων λειτουργούν σαν γέφυρες φέρνοντας κοντά τα Τ κύτταρα φονείς και τα καρκινικά κύτταρα παρά το εχθρικό μικροπεριβάλλον των όγκων, το οποίο παρεμποδίζει αυτή τη διαδικασία οδηγώντας συχνά στην ανθεκτικότητά τους στις θεραπείες».
Τα δικλωνικά αντισώματα της Regeneron δοκιμάζονται αυτή τη στιγμή σε μια πλειάδα κλινικών δοκιμών για συμπαγείς όγκους μεταξύ των οποίων ο καρκίνος του προστάτη και των ωοθηκών. Παρά το γεγονός ότι οι κλινικές δοκιμές για τον προχωρημένο και ανθεκτικό στις υπάρχουσες θεραπείες καρκίνο του προστάτη βρίσκονται ακόμη στη φάση όπου ελέγχεται η ασφάλεια των δικλωνικών αντισωμάτων, τα πρώιμα δεδομένα για την αποτελεσματικότητά τους είναι ενθαρρυντικά: 44% των ασθενών που συμμετείχαν στη μελέτη εμφάνισε μείωση του δείκτη PSA (ενδεικτικός της ύπαρξης καρκίνου του προστάτη), ενώ στο 25% των συμμετεχόντων η μείωση κυμάνθηκε από 82%-100%.
Ερυθηματώδης λύκος
Ο ερυθηματώδης λύκος είναι ένα απειλητικό για τη ζωή (εάν αφεθεί να εξελιχθεί χωρίς φαρμακευτική παρέμβαση) αυτοάνοσο νόσημα το οποίο οι ειδήμονες κατατάσσουν στις ιντερφερονοπάθειες, στις ασθένειες δηλαδή των οποίων η εμφάνιση και η εξέλιξη καθοδηγείται από τις ιντερφερόνες.
Οπως εξήγησε κατά τη διάρκεια της διάλεξής της στο συνέδριο η ισπανικής καταγωγής γιατρός Βιρτζίνια Πασκουάλ (Virginia Pascual), ειδήμων στην παιδιατρική ρευματολογία στο Πανεπιστήμιο Cornell στις ΗΠΑ, «ο συστηματικός ερυθηματώδης λύκος είναι μια πολυγονιδιακή ασθένεια, ενώ η μονογονιδιακή μορφή της εμφανίζεται πολύ νωρίς (συνήθως πριν από το 5ο έτος της ηλικίας) χτυπώντας κατά κύριο λόγο τους νεφρούς και το κεντρικό νευρικό σύστημα».
40 και πλέον μεταλλάξεις σε διαφορετικά γονίδια έχουν συνδεθεί με την εμφάνιση του συστηματικού ερυθηματώδους λύκου
Καθώς πρόκειται για μια ασθένεια με μεγάλη ποικιλία εκφάνσεων (πλήττει διαφορετικούς ιστούς, από το δέρμα και τις αρθρώσεις μέχρι τους πνεύμονες, τους νεφρούς, τον εγκέφαλο, τα αιμοφόρα αγγεία…), η οποία, όπως συμβαίνει συχνά με τα αυτοάνοσα νοσήματα, χαρακτηρίζεται από εξάρσεις και υφέσεις, η κυρία Πασκουάλ και οι συνεργάτες της αξιοποίησαν την τελευταία λέξη της τεχνολογίας προκειμένου να δημιουργήσουν προφίλ των ασθενών τους. Να εξετάσουν δηλαδή όσες το δυνατόν περισσότερες παραμέτρους που χαρακτήριζαν την ασθένεια καθενός από αυτούς.
Κατάφεραν έτσι να κατατάξουν τους ασθενείς σε 7 διαφορετικές κατηγορίες και να εντοπίσουν τα μόρια-κλειδιά τα οποία καθοδηγούν τις εξάρσεις σε κάθε κατηγορία. Προφανώς τα μόρια αυτά αποτελούν κατάλληλους στόχους φαρμακευτικών παρεμβάσεων, οι οποίες μάλιστα θα είναι κομμένες και ραμμένες στις ιδιαιτερότητες των ασθενών.
Νέες ελπίδες
Δεν χωρεί αμφιβολία ότι η σημερινή εμβάθυνση στα μοριακά μυστικά των ασθενειών θα οδηγήσει στα φάρμακα του αύριο. Ωστόσο δεν μπορέσαμε να μη ρωτήσουμε την ισπανίδα ειδήμονα κατά τη διάρκεια κατ’ ιδίαν συνομιλίας μετά τη διάλεξή της για το τι συμβαίνει τώρα με την αντιμετώπιση αυτών των ασθενών και αν υπήρχε ένα ελπιδοφόρο μήνυμα για αυτούς.
«Κατ’ αρχάς είναι ελπιδοφόρο το γεγονός ότι σε σχέση με το παρελθόν τα υπάρχοντα φάρμακα πετυχαίνουν να κρατούν τη νόσο υπό έλεγχο στην πλειονότητα των περιπτώσεων. Ωστόσο, το πλέον ελπιδοφόρο μήνυμα για την αντιμετώπιση του συστηματικού ερυθηματώδους λύκου προήλθε από μελέτη συναδέλφων και αφορούσε τη θεραπεία της νόσου με την αξιοποίηση της τεχνικής των CAR-T κυττάρων».
140 φαρμακευτικά σκευάσματα έχουν αναπτυχθεί από τη μελέτη των κυτταροκινών
Η παραπάνω τεχνική συνίσταται στην απομόνωση Τ κυττάρων από τους ασθενείς, στην κατάλληλη γενετική τροποποίησή τους, στον πολλαπλασιασμό σε συνθήκες εργαστηρίου των γενετικά τροποποιημένων κυττάρων και στη συνέχεια στην επαναχορήγησή τους στους ασθενείς. Η τεχνική, η οποία προϋποθέτει τη χορήγηση χημειοθεραπείας προκειμένου να κατασταλεί το ανοσοποιητικό σύστημα των ασθενών πριν από τη χορήγηση των κυττάρων, αναπτύχθηκε αρχικά για την αντιμετώπιση αιματολογικών καρκίνων.
Ωστόσο «πέρυσι δοκιμάστηκε σε 5 ασθενείς με ερυθηματώδη λύκο (τέσσερις γυναίκες και έναν άνδρα) των οποίων η νόσος δεν μπορούσε να ελεγχθεί με καμιά από τις γνωστές θεραπείες και τα αποτελέσματα ήταν πέρα από κάθε προσδοκία. Η νόσος όχι μόνο ελέγχθηκε, αλλά επετεύχθη δραματική ύφεση η οποία διαρκεί μέχρι σήμερα χωρίς να απαιτείται λήψη φαρμάκων» σημείωσε η δρ Πασκουάλ και πρόσθεσε ότι «βεβαίως ο αριθμός των ασθενών είναι μικρός και βεβαίως αυτοί θα πρέπει να παρακολουθούνται ακόμη. Και ενώ η εν λόγω θεραπεία δεν είναι ενδεδειγμένη παρά μόνο για τις δύσκολες περιπτώσεις, δεν μπορεί να αρνηθεί κανείς ότι πρόκειται για ένα πραγματικά ελπιδοφόρο επίτευγμα».
Ας ελπίσουμε ότι στο εγγύς μέλλον θα έχουμε και άλλα τέτοια ελπιδοφόρα επιτεύγματα.
Ανοσομεταβολισμός: ένα νέο πολλά υποσχόμενο πεδίο
Ενα από τα απολαυστικότερα πράγματα στα συνέδρια είναι το να παρακολουθεί κανείς την εξέλιξη των ιδεών. Το να βλέπει, δηλαδή, σε πραγματικό χρόνο το πώς τα πειραματικά ευρήματα αλλάζουν τη θεώρηση των επιστημόνων για κάποια πράγματα και τους οδηγούν στη δημιουργία νέων υποθέσεων και θεωριών οι οποίες στη συνέχεια θα αποδειχθούν σωστές ή λανθασμένες από την πειραματική διαδικασία.
Περισσότερες από μια φορές έγινε αυτό στη διάρκεια του συνεδρίου της Διεθνούς Εταιρείας Κυτταροκινών και Ιντερφερονών, αλλά επιλέξαμε να σταθούμε σήμερα στην υπόθεση του Λιουκ Ο’ Νιλ (Luke O’ Neill), καθηγητή Βιοχημείας στο Κολέγιο Τρίνιτι στο Δουβλίνο της Ιρλανδίας (ο οποίος εκτός από διακεκριμένος ανοσολόγος είναι και ιδιαίτερα αγαπητός συγγραφέας εκλαϊκευτικών της επιστήμης βιβλίων).
13 μόνο επιστημονικά άρθρα για τον ανοσομεταβολισμό υπήρχαν στη βιβλιογραφία το 2013
Ο Ο’ Νιλ και οι συνεργάτες του διερευνούν τα του μεταβολισμού και η υπόθεση του ιρλανδού καθηγητή είναι ότι η αιτιολογία μιας σειράς ασθενειών έχει τη ρίζα της στη διάρρηξη μιας ενδοσυμβιωτικής σχέσης 2,5 δισεκατομμυρίων ετών! Τότε τοποθετείται χρονικά η είσοδος ενός μονοκύτταρου μικροοργανισμού στον πρόδρομο (μονοκύτταρο τότε) των πολυκύτταρων οργανισμών. Με άλλα λόγια, τότε θεωρούν οι εξελικτικοί βιολόγοι ότι ένας μεγάλος μονοκύτταρος οργανισμός «κατάπιε» έναν μικρότερο, ο οποίος όμως ήταν πολύ αποτελεσματικότερος στο να παράγει ενέργεια από την τροφή του.
Ετσι προέκυψε μια επωφελής και για τους δύο συνεργασία: ο μεγάλος παρείχε την τροφή, την οποία ο μικρός αξιοποιούσε αποτελεσματικότερα και απέδιδε στον μεγάλο το ενεργειακό μερίδιό του. Βαθμηδόν, με το πέρασμα δηλαδή εκατοντάδων χιλιάδων ετών, ο μικρός απώλεσε το μεγαλύτερο μέρος του δικού του γενετικού υλικού και εξελίχθηκε σε ένα από τα σημαντικότερα οργανίδια των κυττάρων, το μιτοχόνδριο.
Οπως λένε τα εγχειρίδια Βιολογίας, τα μιτοχόνδρια αποτελούν τα «εργοστάσια παραγωγής ενέργειας των κυττάρων». Στην πράξη αυτό σημαίνει ότι στα μιτοχόνδρια λαμβάνει χώρα το τελικό στάδιο της αποικοδόμησης των ουσιών που λαμβάνουμε από τη διατροφή μας προκειμένου να παραχθεί η απαιτούμενη ενέργεια για την επιβίωση των κυττάρων μας (και κατ’ επέκταση τη δική μας). Αυτό επιτυγχάνεται μέσω μιας διαδικασίας 8 αντιδράσεων (κύκλος Krebs) οι οποίες καταλύονται από ένζυμα και οι οποίες δίνουν ενδιάμεσα μεταβολικά προϊόντα.
Χαρακτηριστικό παράδειγμα
Κατά τη διάρκεια της διάλεξής του ο ιρλανδός καθηγητής περιέγραψε την αδιάρρηκτη σχέση του μεταβολισμού με το ανοσοποιητικό σύστημα. Χαρακτηριστικό παράδειγμα είναι το ιτακονικό οξύ, το οποίο υπό κανονικές συνθήκες δεν παράγεται ως ενδιάμεσο μεταβολικό προϊόν του κύκλου Krebs, αλλά του οποίου η σύνθεση πυροδοτείται με τη βοήθεια κυτταροκινών από τα μακροφάγα κύτταρα του ανοσοποιητικού συστήματος.
3.380 άρθρα για τον ανοσομεταβολισμό υπήρχαν στις 17 Οκτωβρίου 2023, γεγονός που δείχνει την ανάπτυξη του πεδίου αυτού
Και έχουν κάθε λόγο τα μακροφάγα να κινητοποιούν την παραγωγή ιτακονικού οξέος καθώς αυτό βρέθηκε να έχει αντιμικροβιακή δράση (ενάντια σε βακτήρια όπως ο χρυσίζων σταφυλόκοκκος και ο βάκιλος της φυματίωσης, αλλά και ιούς όπως ο Zika, ο SARSCoV-2 και ο ιός της γρίπης). Το ιτακονικό οξύ βρέθηκε να ασκεί συνολικά τρεις δράσεις που σχετίζονται με το ανοσοποιητικό σύστημα.
Εκτός λοιπόν από την αντιμικροβιακή, έχει και αντιφλεγμονώδη δράση (διαπιστώθηκε ότι εμπλέκεται σε ασθένειες όπως η οστεοαρθρίτιδα, ο συστηματικός ερυθηματώδης λύκος, η ψωρίαση, το άσθμα, ο διαβήτης τύπου Ι, η πολλαπλή σκλήρυνη).
Αλλά και δράση ενάντια στην παχυσαρκία. Μάλιστα μια νέα κατηγορία φαρμακευτικών σκευασμάτων ενάντια στην παχυσαρκία, τα οποία κυκλοφορούν ήδη, βασίστηκε στη δράση του ιτακονικού οξέος, ενώ κλινικές δοκιμές αντιφλεγμονωδών σκευασμάτων «εμπνευσμένων» από το ιτακονικό οξύ είναι καθ’ οδόν.
Μια θεωρία γεννιέται
Αν ένα μόνο μεταβολικό προϊόν μπορεί να ασκεί τόσες δράσεις, μπορεί κανείς να φανταστεί τι θα μπορούσε να συμβαίνει και με τα υπόλοιπα. Ιδιαιτέρως όταν η δράση κάποιων από αυτά μπορεί να είναι και ενισχυτική της φλεγμονής. Σύμφωνα με τον ιρλανδό καθηγητή, «η συστηματική χρόνια φλεγμονή είναι στη ρίζα της αιτιολογίας των καρδιαγγειακών νοσημάτων, του καρκίνου και των αυτοάνοσων νοσημάτων. Εκτιμούμε ότι η μιτοχονδριακή δυσλειτουργία είναι κομβική στην πυροδότηση της χρόνιας συστηματικής φλεγμονής».
Με την υπόθεση του Ο’ Νιλ φαίνεται να συμφωνούν και άλλοι ερευνητές. Η κορυφαία στην παιδιατρική ρευματολογία Βιρτζίνια Πασκουάλ (Virginia Pascual) παρουσίασε ευρήματα τα οποία δείχνουν ότι τα ερυθρά αιμοσφαίρια των ασθενών με ερυθηματώδη λύκο διατηρούν τα μιτοχόνδριά τους (πράγμα που δεν συμβαίνει σε κανονικές συνθήκες καθώς τα ώριμα ερυθρά αιμοσφαίρια δεν είναι παρά «σακουλάκια» με αιμοσφαιρίνη) και εξήγησε ότι «τα ερυθρά αιμοσφαίρια αναγνωρίζονται από τα αντισώματα που έχουν αυτοί οι ασθενείς και έτσι οδηγούνται στο να καταπίνονται από τα μακροφάγα κύτταρα.
Η παρουσία του μιτοχονδριακού DNA μέσα στα μακροφάγα πυροδοτεί τη χαρακτηριστική για την νόσο φλεγμονώδη αντίδραση. Μάλιστα η ένταση των συμπτωμάτων των ασθενών είναι ανάλογη με τα ποσά των μιτοχονδρίων που διατηρούνται στα ερυθρά αιμοσφαίριά τους».
Καινούργια ευρήματα, όπως τα παραπάνω, που αλλάζουν την οπτική των επιστημόνων για την αιτιολογία των ασθενειών έχουν άμεσες συνέπειες στο ευ ζην των ασθενών. Είναι χαρακτηριστικό ότι υπάρχουν ήδη φάρμακα τα οποία στοχεύουν προϊόντα του μεταβολισμού, ενώ μια σειρά νέων φαρμάκων τα οποία θα επιδρούν τόσο σε αυτά όσο και στο μιτοχονδριακό γενετικό υλικό βρίσκονται ήδη σε φάση ανάπτυξης.