Θα ήταν αδύνατον να διανοηθούμε τη ζωή, τουλάχιστον όπως την ξέρουμε, χωρίς την ύπαρξη κυτταρικών διαιρέσεων. Από τις διαιρέσεις του γονιμοποιημένου ωαρίου παράγεται ένα τέλειο έμβρυο, αλλά και χάρη στις διαιρέσεις των κυττάρων ανανεώνονται οι ιστοί στα ενήλικα άτομα. Και βεβαίως, ο καρκίνος εμφανίζεται όταν κάτι στραβώνει με τον έλεγχο των κυτταρικών διαιρέσεων. Δεν είναι λοιπόν περίεργο που η κυτταρική διαίρεση, η «μίτωση» στη γλώσσα των βιολόγων, μπήκε πολύ νωρίς στο ερευνητικό στόχαστρο: εδώ και αιώνες η κυτταρική βιολογία μάς έχει χαρίσει εξαιρετικές εικόνες της μίτωσης και έχει, στην πορεία, διαλευκάνει τα στάδιά της. Ποτέ ωστόσο οι επιστήμονες δεν είχαν καταφέρει να αυξήσουν τόσο τη διακριτική ικανότητα των τεχνικών τους ώστε να μπορούν να παρατηρούν καθεμία πρωτεΐνη που εμπλέκεται στη μίτωση. Αυτό κατέστη δυνατό μόλις πρόσφατα χάρη στην κοπιώδη εργασία του Jan Ellenberg (Γιαν Ελενμπεργκ) και των συνεργατών του στο Ευρωπαϊκό Εργαστήριο Μοριακής Βιολογίας (European Molecular Biology Laboratory, EMBL) στη Χαϊδελβέργη της Γερμανίας.
Τα γονίδια της μίτωσης
Στην πραγματικότητα, το επίτευγμα του Ελενμπεργκ αποτελεί το επιστέγασμα μιας μακρόχρονης ερευνητικής πορείας και υλοποιήθηκε χάρη στις τεράστιες τεχνολογικές προόδους των τελευταίων ετών. Οι τακτικοί αναγνώστες του ΒΗΜΑ-Science θα θυμούνται ίσως τις αναφορές μας στο πρόγραμμα Mitocheck για το οποίο εργάστηκαν πολλοί ερευνητές από διαφορετικές χώρες. Στόχος αυτού του προγράμματος, μέλος του οποίου ήταν και ο Ελενμπεργκ, ήταν να εντοπιστούν τα γονίδια εκείνα που εμπλέκονται (ή/και ελέγχουν) τη μίτωση. Το πρόγραμμα υπήρξε απολύτως επιτυχές: όπως είχε αναφερθεί σε σχετικό άρθρο στην επιθεώρηση «Nature» το 2010, ανάμεσα στα 20.000 και πλέον γονίδια του ανθρωπίνου γονιδιώματος οι ερευνητές είχαν πετύχει να εντοπίσουν τα περίπου 600 που έχουν ρόλο στη μίτωση.
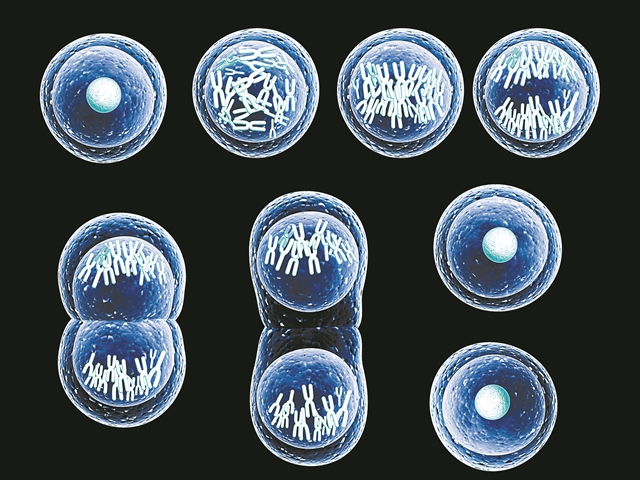
Το ότι ένας τόσο μεγάλος αριθμός γονιδίων εμπλέκεται στη μίτωση δείχνει τη σημασία αλλά και την περιπλοκότητα της διαδικασίας. Μπορούμε να φανταστούμε το κύτταρο σαν ένα φοδραρισμένο πουγκί (καθώς η εξωτερική μεμβράνη του είναι διπλή) μέσα στο οποίο είναι φυλαγμένα όλα τα απαραίτητα οργανίδια για τη λειτουργία του, ενώ στο κέντρο του υπάρχει ένα μικρότερο επίσης φοδραρισμένο πουγκάκι, ο πυρήνας, στο οποίο φυλάσσεται το γενετικό υλικό μας. Σε κάθε μίτωση το μητρικό κύτταρο πρέπει να μοιράσει εξίσου το πολύτιμο φορτίο του: όλα τα οργανίδια πρέπει να διανεμηθούν ισόποσα στα δύο θυγατρικά κύτταρα, ενώ το «ύφασμα και η φόδρα» του πυρήνα πρέπει να αποσυντεθούν προκειμένου να καταστεί δυνατό και το μοίρασμα του γενετικού υλικού. Το οποίο γενετικό υλικό θα έχει εν τω μεταξύ διπλασιαστεί (προκειμένου κάθε θυγατρικό κύτταρο να λάβει ένα ολόκληρο γενετικό αντίγραφο) και θα έχει συμπυκνωθεί σε χαρακτηριστικές δομές, τα χρωμοσώματα. Για τη μεταφορά των χρωμοσωμάτων από το κέντρο του μητρικού κυττάρου προς τα άκρα του δημιουργείται η άτρακτος, μια ειδική δομή του κυτταροσκελετού, ενώ μετά την ολοκλήρωση της διαδικασίας οι δύο θυγατρικοί πυρήνες συντίθενται γύρω από το γενετικό υλικό.
Οι πρωτεΐνες στο προσκήνιο
Καλά είναι τα γονίδια, αλλά τη δουλειά την κάνουν πάντα οι πρωτεΐνες! Αυτό φαίνεται πως σκέφθηκε ο Ελενμπεργκ, ο οποίος τα τελευταία οκτώ χρόνια πραγματοποίησε έναν αληθινό άθλο: δημιούργησε τον πρώτο διαδραστικό πρωτεϊνικό άτλαντα της μίτωσης (Mitotic Cell Atlas). Αναζητήσαμε τον δρα Ελενμπεργκ στο εργαστήριό του στη Χαϊδελβέργη αλλά όπως ενημερωθήκαμε βρισκόταν καθ’ οδόν προς Αυστραλία. Ετσι συνομιλήσαμε με τη στενή συνεργάτριά του δρα Στέφανι Αλεξάντερ (Stephanie Alexander) προκειμένου να αντιληφθούμε καλύτερα όσα αναφέρονται στο τελευταίο άρθρο της γερμανικής ερευνητικής ομάδας το οποίο δημοσιεύθηκε στις 10 Σεπτεμβρίου στον διαδικτυακό τόπο της επιθεώρησης «Nature».
Σύμφωνα με τη δρα Αλεξάντερ, «το πρώτο βήμα για τη δημιουργία του Ατλαντα ήταν να αναπτύξουμε και να βελτιστοποιήσουμε τις τεχνικές που θα επέτρεπαν τη δημιουργία του». Τα σχεδόν 600 γονίδια που εμπλέκονται στη μίτωση κωδικοποιούν για τη σύνθεση ισάριθμων πρωτεϊνών και το ζητούμενο είναι να διαλευκανθεί ο ρόλος τους, κάτι που δεν είναι εύκολο. Ετσι οι ερευνητές ξεκίνησαν από πρωτεΐνες με γνωστό ρόλο, προκειμένου να ρυθμίσουν τις τεχνικές τους. Ολόκληρος ο πειραματισμός έγινε με την κυτταρική σειρά HeLa. Πρόκειται για την παλαιότερη και ως εκ τούτου γνωστότερη στους επιστήμονες ανθρώπινη κυτταρική σειρά. Ελήφθη το 1951 από τη Henrietta Lacks, ασθενή με καρκίνο του τραχήλου της μήτρας, και τα κύτταρα, ως καρκινικά, έχουν την τάση να διαιρούνται συνεχώς. Αποτελούν λοιπόν ένα ιδανικό υλικό για να μπορέσει κανείς να μελετήσει την κυτταρική διαίρεση.
Αυτοματοποιημέναπειράματα
Το πρώτο βήμα του πειραματισμού ήταν η σήμανση της όποιας πρωτεΐνης επρόκειτο να μελετηθεί. Για την ακρίβεια, οι ερευνητές χρησιμοποίησαν την τεχνολογία του «μοριακού ψαλιδιού» (CRIAPR/Cas) προκειμένου να καταστήσουν φωσφορίζουσα την πρωτεΐνη αυτή, ενώ στη συνέχεια παρακολουθούσαν με τη βοήθεια συνεστιακού μικροσκοπίου την κυτταροκαλλιέργεια. Οπως εξήγησε η δρ Αλεξάντερ, «το μικροσκόπιο αυτό είναι εξαιρετικά ευαίσθητο. Στην αρχή όμως δεν χρειάζεται μεγάλη ευαισθησία. Τα κύτταρα παρακολουθούνται και μόλις εντοπιστεί κάποιο που μπαίνει σε φάση διαίρεσης εστιάζουμε σε αυτό. Η όλη διαδικασία είναι αυτοματοποιημένη, ενώ παράλληλα γίνεται και βιντεοσκόπηση».
Καθώς το συνεστιακό μικροσκόπιο επιτρέπει την παρακολούθηση ζωντανού υλικού (εν προκειμένω κύτταρα σε καλλιέργεια) και μπορεί να λαμβάνει εικόνες σε πολλαπλά επίπεδα (κάπως αντίστοιχα με την αξονική τομογραφία), ενώ οι προς μελέτη πρωτεΐνες φωσφορίζουν, οι ερευνητές μπορούν να πληροφορηθούν σε ποιο σημείο του κυττάρου ακριβώς βρίσκεται και πώς αυτή συμπεριφέρεται σε όλη τη διάρκεια της μίτωσης. Επιπροσθέτως, η ευαισθησία του μικροσκοπίου είναι τέτοια που μπορεί εκτός από ποιοτικές να δώσει και ποσοτικές παραμέτρους. Ετσι οι ερευνητές μπορούν να γνωρίζουν αν μια ορισμένη στιγμή σε μια ορισμένη θέση του κυττάρου υπάρχουν 100, 1.000 ή 10.000 πρωτεϊνικά μόρια. Η πληροφορία αυτή είναι πολύ σημαντική, καθώς οι πρωτεΐνες συνεργάζονται, δημιουργώντας συχνά σύμπλοκα μόρια. Οταν λοιπόν αναζητείται ο ρόλος μιας από αυτές, είναι ζωτικό να γνωρίζει κανείς τους συνεργάτες της, καθώς επίσης τον τόπο και τον χρόνο όπου λαμβάνει χώρα η συνεργασία.
Για τη δημιουργία του Ατλαντα μελετήθηκαν 28 πρωτεΐνες-κλειδιά της μιτωτικής διαδικασίας και τα δεδομένα που ελήφθησαν ενσωματώθηκαν σε ένα διαδραστικό υπολογιστικό μοντέλο, η δημιουργία του οποίου υπήρξε και η πλέον χρονοβόρος διαδικασία του ερευνητικού προγράμματος. Και ενώ η γερμανική ερευνητική ομάδα προσθέτει συνεχώς πληροφορίες (και για άλλες πρωτεΐνες), το λογισμικό και όλα τα μεθοδολογικά πρωτόκολλα είναι ανοιχτά για όλους τους επιστήμονες, σε οποιαδήποτε γωνιά του πλανήτη και αν εργάζονται. Επιπροσθέτως, ο Γιαν Ελενμπεργκ και οι συνεργάτες του εκτιμούν ότι οι ίδιες τεχνικές μπορούν να αξιοποιηθούν για την οπτικοποίηση σε πραγματικό χρόνο και άλλων κυτταρικών διεργασιών, όπως παραδείγματος χάριν ο κυτταρικός θάνατος ή η κυτταρική μετανάστευση (προϋπόθεση των μεταστάσεων). Ολα δείχνουν ότι οι γερμανοί επιστήμονες άνοιξαν ένα πεδίο που έχει όλες τις προϋποθέσεις να ανθήσει και να καρποφορήσει στο μέλλον.